Die Beurteilung des Vitamin-D-Status im Körper erfolgt durch die Bestimmung des 25-Hydroxy-Vitamin D und kann wie folgt eingeteilt werden:
• suffiziente Versorgung (>75nmol/l),
• insuffiziente Versorgung (50–75nmol/l),
• Vitamin-D-Mangel (<50 bis 25nmol/l),
• schwerer Vitamin-D-Mangel (<25nmol/l).
Osteoporose - Sinnvolle Labordiagnostik
Die klinische Bedeutung der Osteoporose für Patientinnen und Patienten liegt im Auftreten von Knochenbrüchen und deren Folgen. Die WHO (1994) definiert eine Osteoporose operational durch das Vorliegen eines verminderten Knochenmineralgehalts in einer DXA-Knochendichtemessung an der Lendenwirbelsäule und/oder am proximalen Femur. Die nachfolgende Zusammenstellung berücksichtigt die Osteoporose-Leitlinie 2017 (Langfassung) des Dachverbands Osteologie zur Prophylaxe, Diagnostik und Therapie der Osteoporose im Erwachsenenalter (www.dv-osteologie.de).
Die Prävalenz der Osteoporose hängt vom Alter ab und beträgt bei postmenopausalen Frauen im Alter von 50 bis 60 Jahren ca. 15% und steigt bei >70-jährigen Frauen auf 45% an. Bei Männern beträgt die Prävalenz im Alter von 50 bis 60 Jahren 2,4% und steigt bei >70-jährigen Männern auf 17% an. Die Inzidenz von Knochenfrakturen, das heißt Wirbelkörperfrakturen unter Alltagstätigkeiten und meistens sturzbedingten nicht-vertebralen Knochenbrüchen, nimmt mit dem Lebensalter exponentiell zu.
Zum Beispiel wurde auf Basis Schweizer Daten die Lebenszeitwahrscheinlichkeit für eine größere osteoporotische Fraktur (Oberarm-, Unterarm-, Wirbelkörper- oder Hüftfraktur) bei einem 50-jährigen Mann auf 20,2% und bei einer 50-jährigen Frau auf 51,3% geschätzt.
Klinische Symptome der Osteoporose, die Frakturen vorausgehen, sind nicht sicher beschrieben. Daher ist eine Früherkennung der Störung des Knochenstoffwechsels durch labormedizinische Diagnostik sowie einer verminderten Knochenmineralisation durch DXA-Knochendichtemessung entscheidend, um mit präventiven physikalischen und medikamentösen Therapien das Auftreten von Knochenbrüchen möglichst zu verhindern.
Höheres Lebensalter, weibliches Geschlecht, bereits aufgetretene Knochenbrüche bei manifester Osteoporose und eine Familienanamnese für Frakturen aufgrund von Osteoporose sind Risikofaktoren für osteoporotische Frakturen. Ebenso spielen wiederholte Stürze, insbesondere bei zunehmender Immobilität und Abnahme der Handgriffstärke im Alter, sowie eine verminderte Aufnahme von Calcium mit der Nahrung und eine Hyponatriämie eine Rolle. Rauchen und die damit verbundene COPD sowie Untergewicht (BMI < 20) sind vermeidbare Risikofaktoren für osteoporotisch bedingte Frakturen – umgekehrt schützt ein erhöhter BMI allerdings nicht gegen Frakturen.

Der Zusammenhang zwischen Knochenbrüchen und Stürzen klingt zwar banal, ist aber entscheidend auch für präventive Maßnahmen im Alter. So wird bei Menschen, die älter als 70 Jahre sind, empfohlen, jährlich eine Sturzanamnese zur Feststellung des Sturzrisikos zu erheben. Auch Epilepsie und die Einnahme von Antiepileptika gelten als Risikofaktor für das Auftreten von Knochenbrüchen. Folgende Medikamente sind bei chronischer Einnahme ebenfalls ein Risikofaktor: Protonenpumpeninhibitoren, Glitazone, Aromatasehemmer und hoch dosierte Glukokortikoide. Auch Marcumar und Heparine können den Knochenstoffwechsel negativ beeinflussen.
Als Erkrankungen sind die rheumatoide Arthritis und der Morbus Bechterew jeweils mit einem mäßigen Risiko für osteoporotische Frakturen verbunden. Eine Herzinsuffizienz und auch eine Zöliakie sollten als mäßiger Faktor in die Risikovorhersage von Knochenbrüchen einbezogen werden. Das Risiko für die Entstehung einer Osteoporose und die damit verbundenen Frakturen kann durch hormonelle Störungen erhöht sein – auch bereits in jüngeren Lebensjahren. Diabetes mellitus Typ 1 und Typ 2 stellen einen starken bzw. mäßigen Risikofaktor für das Auftreten von Knochenbrüchen dar. Ein Hyperkortisolismus beispielsweise bei einem Cushing-Syndrom oder einem Nebennierenadenom ist bei Frauen und Männern mit einem sehr starken Risiko für Frakturen verbunden. Die Einnahme relativ hoher Glukokortikoid-Dosen (>7,5 mg Prednisonäquivalent) stellt ebenfalls ein sehr hohes Risiko für Frakturen dar. Auch ein Mangel an Wachstumshormonen bei Hypophyseninsuffizienz sowie eine Hyperthyreose sind mit vermehrtem Auftreten von Knochenbrüchen verbunden. Ein (primärer) Hyperparathyreoidismus ist ebenfalls als ein starker Risikofaktor für Frakturen erwiesen.
Für den Calcium- und Knochenstoffwechsel ist insbesondere auch das hormonell wirksame Vitamin D sehr wichtig.
Ein 25-Hydroxy-Vitamin-D-Serumspiegel von <50 nmol/l ist mit einem mäßig erhöhten Risiko für proximale Femurfrakturen und nicht-vertebrale Knochenbrüche verbunden (relatives Risiko ca. 1,5 bis 2-fach). Frauen haben generell bei gleichem Lebensalter ein etwa 2-fach höheres Risiko für osteoporotische Frakturen als Männer. Im Hinblick auf den Einfluss eines Vitamin-D-Mangels auf die Entstehung einer Osteoporose ist zu bedenken, dass der Knochenstoffwechsel relativ langsam verläuft und unter Umständen eine bereits im jüngeren Lebensalter bestehende Vitamin-D-Mangelsituation die Knochendichte langfristig negativ beeinflussen kann.
In einer durch die LADR unter der Leitung von Prof. Dr. Jan Kramer durchgeführten wissenschaftlichen Studie konnte bestätigt werden, dass in Deutschland in allen Altersgruppen– insbesondere im Jugend- und jungen Erwachsenenalter – ein schwerer Vitamin-D-Mangel (<25 nmol/l) bei ca. 30% der untersuchten Personen relativ häufig ist (Kramer et al. 2014; Deutsche Medizinische Wochenschrift). Eine hohe Homocystein-Serumkonzentration (beachte: Verwendung eines Spezialröhrchens, S-Monovette Homocystein Best.-Nr. 397699) hat sich in epidemiologischen Studien bei Männern und Frauen als ein mäßiger bis starker Risikofaktor für osteoporotische Frakturen erwiesen.
In Studien war auch ein verminderter Folsäure- und Vitamin-B12-Serumspiegel als diätetisch beeinflussbare Determinante der Homocystein-Konzentration mit der Frakturrate assoziiert. Auch ist dargestellt worden, dass eine B-II-Magenresektion oder Gastrektomie, die ursächlich für einen Vitamin-B12-Mangel sein kann, einen starken Risikofaktor für osteoporotische Frakturen darstellen. Dennoch wird aktuell in der Osteoporose-Leitlinie keine allgemeine Empfehlung zur Bestimmung dieser Laborparameter gegeben.
Es sollte aber bedacht werden, dass Auffälligkeiten des Vitamin-B12- und Folsäurehaushalts präventiv durch Supplementation behoben werden können und eine Vitamin-B12-und/ oder Folsäure-Mangelsituation auch andere relevante Auswirkungen auf die körperliche Gesundheit haben kann. Dabei ist zu beachten, dass die Bestimmung des Vitamin B12 selbst kein ausreichender „Frühmarker“ einer Vitamin-B12-Defizienz ist. Für die Früherkennung einer Vitamin-B12-Mangelsituation kann die Bestimmung anderer Parameter wie Methylmalonsäure, Homocystein und Holotranscobalamin (HoloTC) hilfreich sein.
Diagnostisches und therapeutisches Vorgehen bei V.a. Vitamin-D-Mangel
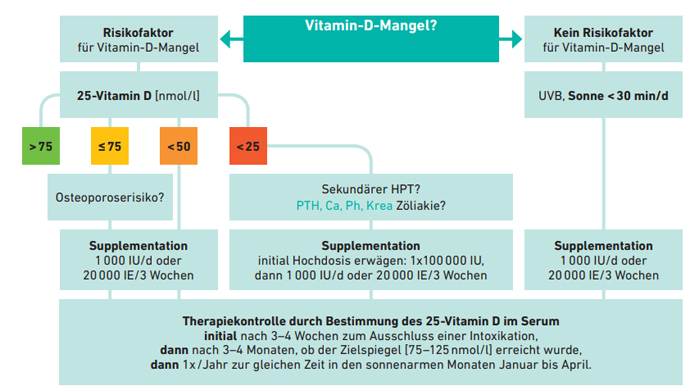
Kramer et al., 2015; DMW · unter Berücksichtigung der DVO-Leitlinie Osteoporose
Empfohlene Bestimmung der Parameter im Basislabor auf Basis der Leitlinie „Osteoporose“
(Langfassung 2017) der Deutschen Gesellschaft für Osteologie
| Basisparameter laut Leitlinie | Bedeutung/Anmerkung | Material |
|---|---|---|
| Calcium | ↑ Primärer Hyperparathyreoidismus oder andere Ursachen einer Hyperkalzämie ↓ z.B. sekundärer Hyperparathyreoidismus (HPT), Malabsorption (MA), Hypokalzämie als Kontraindikation für mehrere Osteoporosemedikamente | Serum |
| Phosphat | Niereninsuffizienz ↑ sekundärer renaler Hyperparathyreoidismus (HPT) ↓ Malabsorption | Serum |
| Natrium | ↓ erhöhtes Risiko für vertebrale und nicht-vertebrale Frakturen | Serum |
| AP (Alk. Phosphatase) | ↑ z.B. Osteomalazie ↓ möglicher Hinweis auf das Vorliegen einer Hypophosphatasie | Serum |
| Gamma-GT | Zur Differentialdiagnose einer hepatisch bedingten AP-Erhöhung, Hinweis auf Zöliakie oder Alkoholabusus (Sturzrisiko) | Serum |
| Kreatinin und Krea-Clearance nach Cockroft-Gault | ↑ renale Osteopathie Höhergradige Niereninsuffizienz als Kontraindikation für verschiedene Medikamente | Serum |
| CRP | ↑ Differentialdiagnose entzündlicher Ursachen von Wirbelkörperdeformitäten, entzündlich-rheumatische Erkrankungen | Serum |
| BSG | ↑ Differentialdiagnose entzündlicher Ursachen von Wirbelkörperdeformitäten, entzündlich-rheumatische Erkrankungen | EDTA |
| Blutbild | Hinweise auf entzündliche und maligne Erkrankungen oder Zöliakie | EDTA |
| Eiweißelektrophorese; freie Kappa- und Lambda-Leichtketten quantitativ sinnvoll | Hinweis für Multiples Myelom (MM) | Serum |
| TSH | <0,3mU/l endogen oder durch L-Thyroxin-Medikation bedingt, als Risikofaktor für Frakturen | Serum |
| Ggf. Testosteron bei Männern; zusätzlich SHBG sinnvoll; morgendliche Abnahme empfohlen | Testosteronmangel | Serum |
| Ggf. 25-Hydroxy-Vitamin D in Einzelfällen (*) | Vitamin-D-Mangel | Serum |
| Ggf. Knochenresorptionsparameter in Einzelfällen (#) | hoher Knochenumbau als Frakturrisiko | Siehe Angabe zu den Parametern unten (#) |
(*) Die Messung von 25-Hydroxy-Vitamin D sollte laut Leitlinie bei Hinweisen auf eine Osteomalazie sowie z.B. bei Personen mit geringer Sonnenlichtexposition, Trägerinnen verhüllender Bekleidung, bei einer Niereninsuffizienz oder bei gastrointestinalen Erkrankungen sowie bei Vitamin-D-Supplementation erfolgen.
(#) Beurteilung des Knochenumsatzes
Knochenresorption:
- β-CTX („CrossLaps“) im EDTA-Plasma; 24h stabil bei Raumtemperatur (nur 8h im Serum); Blutentnahme nüchtern morgens 7–9 Uhr
- „Crosslinks“ im Urin des Knochenkollagens Pyridinolin (PYD) und Desoxy-Pyridinolin (DPD): unabhängig von der Ernährung; stabiler als Serumparameter. Präanalytik: 10ml zweiter Morgenurin, Sonneneinwirkung vermeiden
- TRAP 5b im Serum (stabil bei taggleichem Laboreingang; unabhängig von Ernährung, keine tageszeitliche Schwankung)
Knochenaufbau:
- P1NP (Prokollagen-1-N-terminales Propeptid) im Serum oder im EDTA-Plasma; stabil bei Raumtemperatur
- Ostase (knochenspezifische Alkalische Phosphatase) im Serum; stabil bei Raumtemperatur
- Osteocalcin im EDTA-Plasma; stabil für 2 Tage bei Raumtemperatur (nur 8h im Serum); Blutentnahme nüchtern morgens 7–9 Uhr
Bei Patienten z.B. mit Knochenmetastasen oder -frakturen, Morbus Paget oder Hyperparathyreoidismus werden ebenfalls erhöhte Parameter des Knochenumsatzes gefunden.
Weiterführende und ggf. sinnvolle zusätzliche Laboruntersuchungen bei Verdacht auf Osteoporose(gemäß Leitlinie)
- Calcium im 24-h-Urin (Diagnose der idiopathischen Hyperkalziurie)
- Cadmium im Urin bei unklaren Fällen von Osteoporose. Eine hohe Aufnahme von Cadmium mit der Nahrung ist vor allem bei Nichtrauchern ein mäßiger bis starker Risikofaktor für Frakturen. Aufnahmequelle von Cadmium können kontaminierte Meeresfrüchte (Schalentiere) und grünes Blattgemüse sowie bei Rauchern eben auch Zigaretten sein. Auch arbeitsplatzbezogene Expositionen sind zu berücksichtigen. Der 2007 eingeführte biologische Leitwert für Cadmium im Urin von 7 μg/l wurde zwischenzeitlich wieder zurückgezogen, da die Datenlage zurzeit nicht eindeutig genug ist. Die bestehende Hintergrundbelastung für beruflich nicht Cadmium-exponierte Personen im erwerbsfähigen Alter ist allerdings mit den vorhandenen Biologischen Arbeitsstoff-Referenzwerten (BAR) von 1 μg/l im Blut und 0,8 μg/l im Urin beschrieben und kann als Referenzmaßstab dienen.
| Ggf. sinnvolle zusätzliche weitere Laborparameter: | |
|---|---|
| V.a. Hyperparathyreoidismus | Parathormon i.S. |
| V.a. Hyperkortisolismus | Cortisol i.S. morgens |
| V.a. Östrogenmangel bei Frauen | Östradiol i.S |
| V.a. rheumatoide Arthritis | hs-CRP und anti-CCP i.S. |
| V.a. Morbus Bechterew | HLA-B27 in EDTA-Blut |
| V.a. Herzinsuffizienz | NT-proBNP i.S. |
| V.a. Zöliakie | IgA i.S. in Kombination mit Transglutaminase-/Endomysium-IgA-Ak; bei IgA-Mangel, dann Transglutaminase/Endomysium-IgG-Ak i.S.; deamidierte Gliadinpeptid-Ak i.S.; DQ2 und DQ8 in EDTA-Blut (GenDG beachten) |
| V.a. Vitamin-B12-Mangel | Vitamin B12 i.S., Holotranscobalamin (HoloTC) i.S. |
| V.a. Hyper-Homocysteinämie | Nur Homocystein-Bestimmung im Spezialröhrchen mit saurem Citrat (Best.-Nr. 397699) durchführen. CAVE! Ansonsten muss EDTA- bzw. Vollblut innerhalb von 30min zentrifugiert und das Plasma/Serum sofort abgetrennt werden, um die Freisetzung von Homocystein aus den Erythrozyten zu minimieren. |
| V.a. Folsäuremangel | Folsäure i.S. |
| V.a. Alkoholabusus | Ethylglucuronid i.S. oder im Urin |
| V.a. Unterernährung | Albumin i.S. |
| V.a. Multiples Myelom | Immunfixationselektrophorese und freie Leichtketten i.S. |
-
Analysen
-
Downloads
-
Seminare
-
Konsiliarnetzwerk










































