Gezielte Rhesusprophylaxe - Spritze nur, wenn nötig
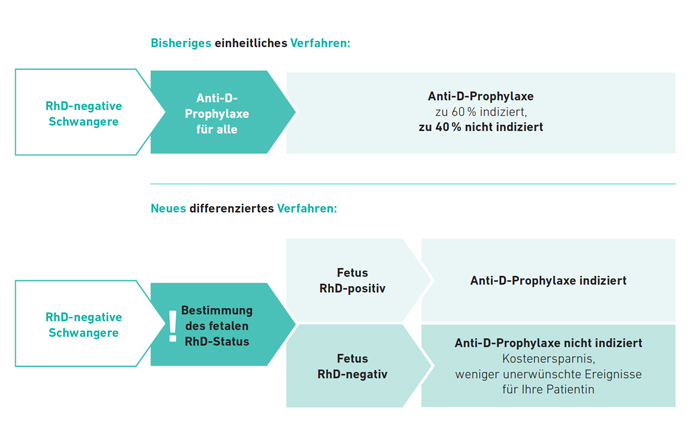
Bereits seit 2017 bieten wir ein sicheres Verfahren zur Bestimmung des fetalen Rhesusfaktors D aus mütterlichem Blut an. Nur im Fall eines RhD-positiven Fetus ist die pränatale Rhesusprophylaxe in der 28. SSW erforderlich.
Bei etwa 40 % der RhD-negativen Schwangeren ist sie dementsprechend überflüssig. Dieser Tatsache trägt der neue G-BA Beschluss, der am 24.11.2020 in Kraft getreten ist, Rechnung.
Zum 1. Juli 2021 wurden die fachgebundene genetische Beratung und die Laboruntersuchung des fetalen Rhesusfaktors D als neue Kassenleistung in den EBM aufgenommen. Die Laborleistung können Sie damit mittels Muster 10 in Ihrem LADR Labor für Ihre GKV-versicherten Patientinnen anfordern.
Begründung für die gezielte Rhesusprophylaxe
Bei den Präparaten zur Prophylaxe handelt es sich um humane Blutprodukte. Blutspendern, die selbst D-negativ sein müssen, wird mehrmals D-positives Blut „transfundiert“. Die in den meisten Fällen nach einigen Wochen gebildeten Antikörper werden mittels Plasmaspende gewonnen, das Plasma wird entsprechend verarbeitet und auf die gängigen Infektionsmarker getestet. Zusätzlich werden Virusinaktivierungsmaßnahmen durchgeführt, welche allerdings nur umhüllte Viren eliminieren.
Abgesehen vom minimalen Restrisiko für die Übertragung von Infektionserkrankungen werden die typischen Nebenwirkungen humaner Immunglobuline beobachtet (Tachykardie, Hypotonie, Anaphylaxie, Übelkeit, Arthralgie), meist in einer Häufigkeit zwischen 1:1.000 und 1:10.000 (Quelle: Fachinformationen Rhophylac 300, CSL Behring). Außerdem sind die Präparate teuer und vor allem nur begrenzt verfügbar bzw. herstellbar.
Die moderne molekulare Fetaldiagnostik erlaubt inzwischen, den RhD-Status des Fetus zuverlässig mittels PCR aus dem Blut der Mutter zu bestimmen. Schon in der 2017 aktualisierten Hämotherapie-Richtlinie findet sich folgende Empfehlung: „Eine Anti-D-Prophylaxe bei der Schwangeren ist nicht notwendig, wenn der Fetus mit einem validierten Verfahren RhD-negativ bestimmt wurde. Nach der Geburt ist das Merkmal RhD, vorzugsweise aus Nabelschnurblut, zu bestimmen."
Das LADR Zentrallabor Dr. Kramer & Kollegen führt seit 2017 die Bestimmung des fetalen RhD-Status mit dem FetoGnost Kit durch. Eine Zusammenfassung der klinischen Studie "Evaluierung des FetoGnost Kit RhD als nicht invasiven Pränataltest zur Bestimmung des fetalen RhD-Status (NIPT-Rhd)" finden Sie im Deutschen Register Klinischer Studien (DRKS).
Gezielte Rhesusprophylaxe: Bedeutung der im GBA-Beschluss verfügten Änderungen für die Praxis
Sie müssen die RhD-negativen Schwangeren über die Möglichkeit der „gesteuerten Prophylaxe“ aufklären. Falls die Schwangere sich dafür entscheidet, schicken Sie uns ab der 12. SSW 6-7,5 ml EDTA-Blut der Schwangeren. Wurde die Blutprobe freitags abgenommen und muss bis Montag in der Praxis bleiben, lagern Sie die Proben bei 4 °C. Auf keinen Fall die Blutprobe einfrieren!

Aufgrund der sehr hohen Sensitivität des RhD-Nachweises ist hier besondere Aufmerksamkeit auf eine mögliche Kontamination zu legen. Daher bitten wir um Einsendung eines separaten Röhrchens für diese Analyse. Wir teilen Ihnen wenige Tage später den Rh-Faktor D des Kindes mit. Falls dieser positiv ist, geben Sie wie gewohnt die Anti-D- Prophylaxe. Falls nicht, verzichten Sie auf die Prophylaxe.
Der günstigste Zeitpunkt für die Bestimmung des fetalen RhD
Der Test ist ab der 12. Woche zugelassen. Die Sicherheit des Nachweises steigt aber vermutlich mit der Schwangerschaftsdauer an, da der Anteil der fetalen DNA im mütterlichen Blut stetig zunimmt (siehe Abbildung unten). Insofern liegt der günstigste Termin für reguläre Schwangerschaften etwa in der 20 SSW, dann ist noch sehr ausreichender Zeitpuffer bis zum Zeitpunkt der Prophylaxe.
Wenn andererseits die Patientin einige Wochen eher ohnehin in der Praxis ist, kann die Abnahme auch bei dieser Gelegenheit durchgeführt werden. Die Möglichkeit, den Test schon in der 12 Woche durchzuführen, ist vor allem für Schwangerschaftskomplikationen interessant, bei denen eine D-Prophylaxe infrage kommt (z.B. EU-Gravidität).
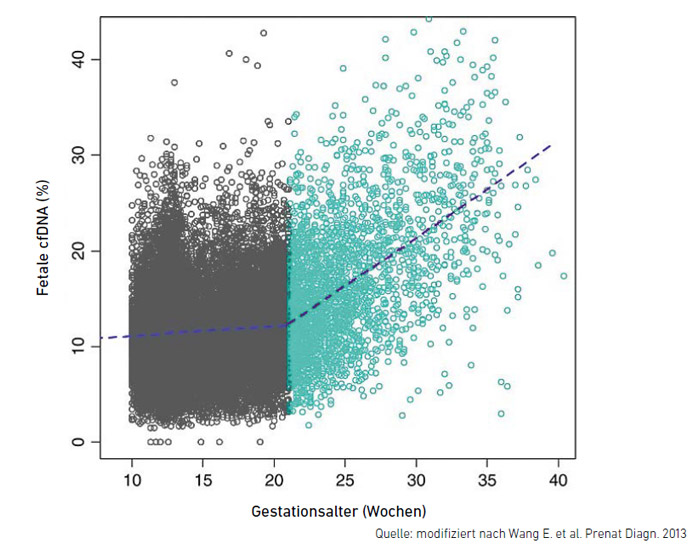

Die Abbildung zeigt: Der Anteil fetaler DNA im mütterlichen Blut nimmt mit der Dauer der Schwangerschaft zu.
Genetische Beratung
Gemäß dem G-BA Beschluss im Rahmen der Mutterschafts-Richtlinien muss die verantwortliche ärztliche Person, die die Schwangere vor und nach Durchführung des NIPT-RhD genetisch berät, über eine Qualifikation für diese Beratung gemäß Gen DG und den Richtlinien der Gendiagnostik-Kommission (fachgebundene genetische Beratung) verfügen.
Abrechnung Rhesusprophylaxe
| Parameter | Probenmaterial | EBM | GOÄ | ||
|---|---|---|---|---|---|
| Ziffer | € | Ziffer | € (1,15-fach) | ||
| Beratung nach GenDG zum NIPT-RhD gemäß Abschnitt C und Anlage 7 der Mutterschaftsrichtlinien | 01788 | 9,34 € (84 Punkte) | |||
| Pränatale Bestimmung des fetalen Rhesusfaktors D an fetaler DNA aus mütterlichem Blut | 6-7,5 ml EDTA-Blut der (RhD-negativen) Schwangeren ab der 12. SSW in einem extra Röhrchen | 01869 | 100,68 € (905 Punkte) | 1 x 3920 1 x 3922 3 x 3924 | 1 x 60,33 € 1 x 33,52 € 3 x 20,11 € (Gesamtsumme = 154,18 €) |
Kostenlose Online-Fortbildung zur gesteuerten Rhesus-Prophylaxe
Anlässlich der Aufnahme der gesteuerten Rhesus-Prophylaxe in den Leistungskatalog der gesetzlichen Krankenversicherung bietet die LADR Akademie eine kostenlose Online-Fortbildung (1 CME-Punkt) zu diesem Thema an. Die Fortbildung gibt einen umfassenden Überblick über aktuelle Aspekte und Hintergründe zum Thema Rhesus-Prophylaxe.
-
Analysen
-
Downloads
-
Seminare